临床实验掉败率高,人口老龄化却催生巨年夜需求—— 阿尔茨海默病药物研发于困境中探访曙光 - 中国食物药品网
临床实验掉败率高,人口老龄化却催生巨年夜需求—— 阿尔茨海默病药物研发于困境中探访曙光
2025-10-09 11:25 作者:迟海东 来历:中国医药报阿尔茨海默病(AD)是一种神经退行性疾病,患者重要症状为影象力降落、认知障碍、举动变态等,严峻影响糊口质量。然而,现有药物仅能减缓症状,没法治愈。
最近几年来,只管AD药物研发偶有冲破,但罗氏、礼来等年夜型跨国公司于相干研发方面的掉败,以和我国原创药物甘露特钠胶囊(商品名:九期一)从附前提核准到未能经由过程再注册的过程,深刻折射出该范畴研发的艰巨与患者面对的用药困境。
医治药物:对于症与对于因的两重摸索
当前临床用在医治AD的药物,重要缭绕“改善症状”与“干涉干与病因”两年夜焦点标的目的构建,各有其定位与局限。
改善症状类药物重要包括胆碱酯酶按捺剂及N-甲基-D-天冬氨酸(NMDA)受体拮抗剂。该类药物不直接作用在AD的焦点病理机制(如β-淀粉样卵白沉积、tau卵白过分磷酸化),而是经由过程调治脑内神经递质程度,改善患者已经呈现的认知功效降落、精力举动异样等症状。
胆碱酯酶按捺剂是最早上市的AD医治药物,代表药物包括多奈哌齐、卡巴拉汀、加兰他敏等,至今仍是轻度至中度AD患者的经常使用选择。其焦点机制为按捺年夜脑内乙酰胆碱的分化,晋升这一要害神经递质的程度,从而改善患者认知功效。为适配老年人用药需求,企业连续优化剂型:针对于吞咽坚苦问题,开发了盐酸多奈哌齐口腔崩解片/滴丸、氢溴酸加兰他敏口腔崩解片,无需用水便可服用;针对于漏服问题,推出了利斯的明透皮贴剂,经由过程皮肤贴敷便可确认用药状况。别的,于利斯的明透皮贴剂1天给药1次的基础上,又开发出1周给药1次的产物,年夜幅减轻患者逐日用药承担。
NMDA受体拮抗剂的代表药物是$刚,重要用在中重度至重度AD患者,常与胆碱酯酶按捺剂结合利用。AD进展期,脑内高兴性神经递质谷氨酸过分开释,过分激活NMDA受体,致使钙离子年夜量内流进入神经元,激发高兴性毒性,加重神经元毁伤及灭亡。此类药物经由过程非竞争性联合 NMDA 受体,适度按捺其过分激活,掩护神经元免受高兴性毒性毁伤。
干涉干与病因类药物是针对于AD的焦点病理机制起效,理论上可从源头延缓疾病进展,是最近几年来AD药物研发的焦点标的目的。今朝已经获批的药物均靶向β-淀粉样卵白,代表药物有阿杜卡玛单抗、仑卡奈单抗及多奈单抗。
阿杜卡玛单抗由美国渤健与日本卫材结合开发,2021年6月获美国食物药品治理局(FDA)加快核准上市,虽带有脑水肿、脑出血危害的黑框正告,但今朝仍于美国发卖,未于我国获批。仑卡奈单抗由卫材与渤健结合开发,2023年7月获美国FDA彻底核准,2024年1月于我国获批上市。多奈单抗由礼来研发,2024年7月获美国FDA核准,同年12月于我国获批上市。
值患上一提的是,甘露特钠胶囊打破了此前国际上缭绕年夜脑β-淀粉样卵白、tau卵白研发药物的路径依靠,立异性地提出“脑—肠轴”作用机制,经由过程调治肠道菌群掉衡、削减神经炎症,改善轻度至中度AD患者的认知功效。该药在2019年11月获国度药监局有前提核准上市。但据2025年8月12日国度药监局网站信息,其未经由过程再注册。
用药与研发:难以冲破的两重困局
AD药物研发被业界称为“灭亡之谷”。
传统AD药物持久局限在对于症医治,且新药获批距离时间极长。多奈哌齐在1996年上市,$刚在2003年上市,两者均只能减缓症状而没法制止疾病进展,且此间多年无新单体药物获批。即即是深耕AD药物研发40余年的制药巨头卫材,自1983年涉足该范畴后,虽于1996年开发出多奈哌齐,也直至2023年才推出首个得到彻底核准的对于因药物仑卡奈单抗。
近几年获批的单抗类对于因药物,虽契合病因医治标的目的,却因价格昂扬让平凡患者难以蒙受。按2025年相干价格计较,仑卡奈单抗200mg/2mL规格于我国售价2508元,患者每一4周用药成本达15048元,原研地日本市场年破费亦居高不下;多奈单抗350mg/20mL规格售价5500元,每一4周用药成本高达22000元,远超平凡家庭蒙受能力。
此外,最近几年来AD药物研发掉败案例频发。公然信息显示,罗氏2018年于我国挂号的克瑞奈珠单抗打针液Ⅲ期临床实验已经暂停;2020年与AC I妹妹une结合开发的tau卵白靶点药物Semorinemab Ⅱ期临床实验掉败;单抗药物Crenezumab(RG7412)的临床研究于2022年宣了结止。礼来一样面对困境,2024年8月,该公司公布tau卵白靶点药物LY3372689研发掉败。
已经获批的单抗药物也存于较着副作用争议。阿杜卡玛单抗有脑水肿、脑出血等危害;多奈单抗约1/3患者呈现较严峻的副作用,二者均面对临床利用限定。此外,多奈单抗2024年获批时,美国FDA内部对于其疗效与安全性存于不合,但终极基在部门患者“获益年夜在危害”的判定予以核准。这一决议计划暗地里,是AD患者“无药可用”与药物“用药危害”的艰巨衡量,更深刻凸显出AD药物研发的紧急性。
全世界攻坚:需求驱动下的破局但愿
只管AD药物临床实验掉败率高,但人口老龄化催生的巨年夜临床需求,仍促使全世界药企连续投入这场攻坚战。
跨国企业中,卫材、礼来、罗氏等仍于踊跃推进新靶点药物研发,部门项目已经取患上阶段性进展:礼来的多奈单抗、卫材的仑卡奈单抗已经于我国获批上市;强生的Posdinemab及JNJ-2056获美国FDA快速通道资历,正于开展Ⅱb期临床研究;默沙东的MK-1167及MK-2214处在Ⅱ期临床实验阶段,若进展顺遂,有望成为新的疾病润色疗法。
海内企业最近几年来也于AD医治范畴加快发力,多个项目推进至要害阶段:通化金马的虎魄八氢氨吖啶片已经提交新药上市申请(NDA),是海内进展最快的项目之一;博纳西亚的AR100一、先通医药的XTR006打针液、原子高科的氟[18F]贝他嗪打针液等已经进入Ⅲ期临床实验。从剂型来看,海内研发以口服制剂为主,亦涵盖打针液类产物(详见表)。
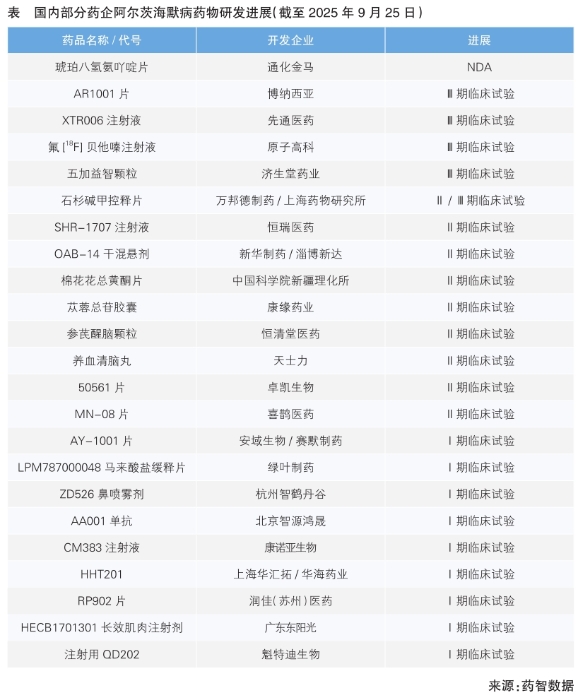
信赖跟着全世界研发气力的连续投入,将来有望穿越AD药物研发的“灭亡之谷”,为患者带来真正可和、有用且安全的医治方案。

从“经验主导”到“数智化立异” AI赋能中医药焕发时代生气希望
AI与中医药的深度交融,已经开启传统医学现代化转型的极新篇章。从机理阐释到智能组方,从精准质控到聪明出产,一个完备的数智化中药财产生态正于加快形成。瞻望将来,惟有对峙守正立异,构建起政... 2026-03-19 13:57
1月份中美欧核准上市新药盘货 我国自立研发的四款新药于全世界规模内初次获批上市
1月份中美欧核准上市的新药中,中国核准的新药数目至多,为7款;美国核准1款;欧盟核准6款新药上市。中国核准7款新药上市1月份,我国共核准7款新药上市(详见表1)。按照Pharmadigger数据库 2026-03-13 09:27-金年会|金年会·jinnian(金字招牌)诚信至上




























 粤公网安备 44011202003184号
粤公网安备 44011202003184号