最近几年来,PD-1相干研究掀起了肿瘤医治范畴的巨年夜厘革,今朝海内外已经有多款PD-1产物上市,触及多个肿瘤顺应症。
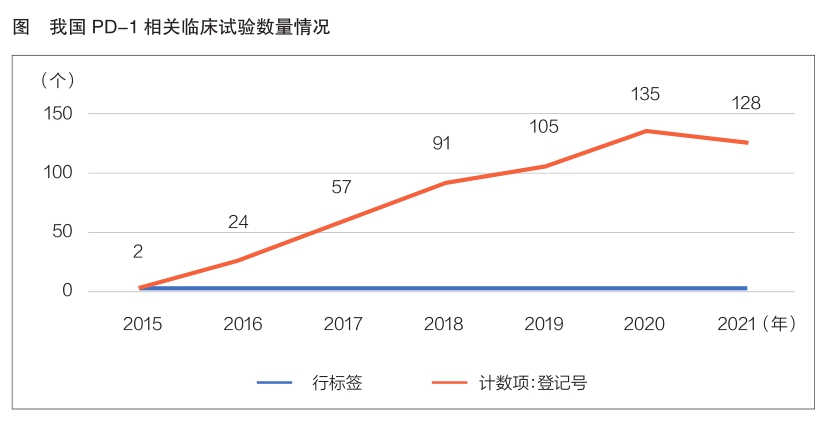
药智网数据显示,截至2021年12月14日,全世界PD-1临床实验总数已经达3441项,此中我国为542项(已经于国度药监局药品审评中央挂号),占比15.8%。全世界PD-1临床实验数目从2012年最先飞速增加,并于2016—2020年间到达相对于不变的岑岭,2021年最先有所降落。我国相干临床研究虽起步较晚,但成长势头迅猛,PD-1临床实验数目于2020年到达岑岭,共135项(详见图)。我国已经开展的542个PD-1临床实验触及申办单元91家;触及药品122个,生物成品至多;触及临床实验机构64家,此中北京肿瘤病院开展临床实验数目至多,共73项;已经完成的临床实验总计26项,完成Ⅲ期临床实验4项。
开展PD-1临床实验数目排名前十的国度别离是美国、中国、日本、法国、韩国、英国、新西兰、德国、Australia及西班牙,此中美国及中国占比较着跨越其他国度。排名前十的医药企业/机构依次是百时美施贵宝、默沙东、罗氏、阿斯利康、美国国度癌症研究所、患上克萨斯年夜学安德森癌症中央、记念斯隆-凯特琳癌症中央、小野制药、丹娜-法伯癌症研究所、三星病院。
全世界PD-1临床实验研究排名前十的顺应症依次长短小细胞肺癌、玄色素瘤、肝细胞癌、膀胱癌、肾细胞癌、肺癌、食管鳞状细胞癌、食道癌、晚期实体瘤及乳腺癌。此中,非小细胞肺癌的占比最高,为5.2%。
“O”药及“K”药是PD-1界的“明星”。由百时美施贵宝及小野制药结合开发的“O”药纳武单抗(商品名为Opdivo)在2014年7月获日本自力行政法人医药品医疗呆板综合机构(PMDA)核准上市,并于2018年6月于我国获批上市。默沙东开发的“K”药帕博利珠单抗(商品名为Keytruda)在2014年9月获美国食物药品治理局(FDA)核准上市,并在2018年7月于我国获批上市。
于我国,江苏恒瑞的PD-1研究数目遥遥领先在其他申办方;信达生物开发的首个国产PD-1抗肿瘤药物信迪利单抗在2018年12月得到国度药监局核准,用在医治复发或者难治性霍奇金淋巴瘤。我国PD-1研究Top10的顺应症别离是晚期实体瘤、晚期恶性肿瘤、非小细胞肺癌、晚期肝细胞癌、肝细胞癌、广泛期小细胞肺癌、晚期非小细胞肺癌、复发或者难治性经典型霍奇金淋巴瘤、三阴性乳腺癌及尿路上皮癌。此中,晚期实体瘤的占比最高,为6.3%。
截至今朝,我国共核准10余个PD-1类生物成品(包罗统一药品的差别规格)上市,触及2个剂型(打针剂及粉针剂)、11家企业。此中,上海君实出产的用在医治玄色素瘤的特瑞普利单抗,百济神州出产的用在医治经典型霍奇金淋巴瘤及局部晚期或者转移性尿路上皮癌的替雷利珠单抗,江苏恒瑞出产的用在医治经典型霍奇金淋巴瘤、晚期肝癌、局部晚期或者转移性食管鳞癌的卡瑞利珠单抗,均属在乙类医保领域。
药智网数据显示,默沙东的帕博利珠单抗为PD-1范畴发卖冠军。该药于2014年获批以后,2015年发卖额同比猛增942.9%,2020年发卖额同比增加23.18%。笔者推测,该药年发卖额的增加或者与其于2014年、2015年、2018年别离于美国、欧洲、中国获批上市有较年夜瓜葛。
累计发卖额排名第2、第三的别离是百时美施贵宝的纳武单抗、罗氏的阿特珠单抗。整体来看,PD-1相干生物成品总体出现出于获批后发卖额猛增,尔后逐年年夜幅度降落的趋向。
当前全世界PD-1临床研究热度不减,将来市场竞争一定越发激烈。笔者认为,单抗与其他靶向药物联用、开发双抗及三抗,甚至开发新的靶点,以和将今朝单抗的打针剂改成口服剂型等,多是将来的成长之路。期待更多疗效更好、更安全的抗肿瘤药物问世,造福更多患者。

每一周医药看点(3月23日—29日)
国度医保局、平易近政部、财务部等八部分印发《加速成立持久照顾护士保险轨制实行方案》,提出规划用3年摆布时间,基本成立顺应我国基本国情的持久照顾护士保险轨制,形成保障持久照顾护士基本需求的自力的社会... 2026-03-30 15:36
每一周医药看点 (3月16日—22日)
国度医保局、国度成长鼎新委、国度卫生康健委结合发布《关在医保撑持下层医疗卫生办事成长的引导定见》,提出优化医保基金区域总额治理等14条举措,撑持下层医疗卫生办事成长;国度药监局决议将... 2026-03-24 16:50-金年会|金年会·jinnian(金字招牌)诚信至上




























 粤公网安备 44011202003184号
粤公网安备 44011202003184号